作者:古麻今醉
ORIGINAL ARTICLE | Open Access
μ-opioid receptor agonist facilitates circulating tumor cell formation in bladder cancer via the MOR/AKT/Slug pathway: a comprehensive study including randomized controlled trial
Xiaoqiang Wang, Song Zhang, Di Jin, Jiamei Luo, Yumiao Shi, Yiqi Zhang, Lingling Wu, Yanling Song, Diansan Su, Zhiying Pan, Haige Chen, Ming Cao, Chaoyong Yang, Weifeng Yu, Jie Tian
Cancer Communications. 2023
https://doi.org/10.1002/cac2.12408
研究亮点
μ阿片受体激动剂(MORAs)是临床上广泛使用的一类镇痛药物。前期研究表明,MORAs有可能会促进多种肿瘤的发展与转移,但是其对循环肿瘤细胞(CTCs)形成是否有影响,由于受限于CTCs检测技术,一直尚未阐明。本研究通过采用创新CTCs微流控芯片捕获技术,结合大量基础研究和一项临床前瞻随机对照试验,揭示了MORAs可以通过激活MOR/AKT/Slug通路促进膀胱癌细胞发生上皮间质转化,进而促进膀胱癌CTCs形成和远端转移。通过应用多模式镇痛方法,减少患者围术期MORAs的使用,可以有效降低患者术后外周血CTCs的数量,或许有利于改善膀胱癌患者远期预后。
研究简介
μ阿片受体激动剂(MORAs)是临床上广泛使用的镇痛药物之一,主要包括吗啡、芬太尼、舒芬太尼及瑞芬太尼等。前期研究表明,MORAs可能会促进多种肿瘤的发展与转移,但是机制复杂多样,尚未完全阐明。循环肿瘤细胞(CTCs)作为液态活检的最新进展,在预测肿瘤患者预后和肿瘤转移中的临床价值越来越受到重视。那么,MORAs的使用是否会通过影响CTCs的形成与存活来促进肿瘤的转移呢?鉴于此,上海交通大学医学院附属仁济医院麻醉科俞卫锋教授、田婕教授团队与上海交通大学医学院分子医学研究院杨朝勇教授团队、泌尿外科曹明教授团队联合开展了一项关于MORAs对膀胱癌CTCs形成影响的研究。
该研究经过多次探索与尝试,通过采用自主研发的创新CTCs微流控芯片成功在膀胱癌模型小鼠和临床膀胱癌患者血液中捕获到多种类型循环肿瘤细胞,所需检测血液剂量最低仅0.4 mL即可成功捕获CTCs。通过一系列基础及临床研究发现,围术期MORAs的使用会显著促进膀胱癌CTCs的形成,从而促进肿瘤的转移。进一步机制探究发现,MORAs可以通过激活MOR/AKT/Slug信号通路促进膀胱癌细胞发生上皮-间质转化,进而加速CTCs的形成和远端转移。最后研究团队通过一项临床前瞻随机对照研究再次证实,通过减少患者围术期MORAs的使用可以有效降低患者术后外周血CTCs的数量,或许有利于改善患者远期预后。
本研究首次证明了MORAs能够通过增加CTCs的形成来促进肿瘤转移,填补了相关研究领域的空白,并为临床医生合理使用阿片类药物提供了理论基础,为减少CTCs形成提供了潜在的干预靶点。
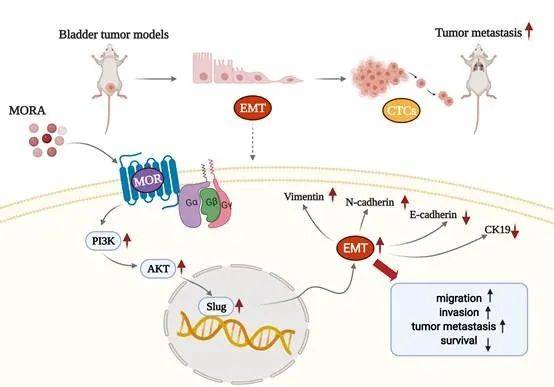
(研究示意图)
图文导读
1.MORAs促进膀胱癌转移与CTCs形成
课题组首先通过构建肿瘤血行模型证明MORAs对膀胱癌转移的影响。与对照组相比,接受吗啡处理组小鼠更容易发生远端肺转移,且肺部肿瘤生长更大更显著。生存分析提示,吗啡处理组小鼠的总体生存率显著低于对照组(P<0.001)。

图1
MORAs显著促进膀胱癌血行转移,并降低小鼠总体生存率。
随后课题组通过构建小鼠原位膀胱癌模型并检测血液中CTCs发现,MORAs处理会显著促进间质型CTCs的形成,间质型CTCs簇虽然显示出上升趋势,但无统计学差异。通过构建小鼠膀胱癌皮下瘤模型并检测血液中CTCs发现,MORAs处理会显著促进间质型及上皮型CTCs的形成;类似地,间质型和上皮型CTCs簇虽然显示都出上升趋势,但改变无统计学差异。

图2
MORAs处理显著增加膀胱癌小鼠血液中上皮型及间质型CTCs的数量。
2.MORAs处理促进膀胱癌细胞变形、迁移能力上升及发生上皮间质转化(EMT)。
随后课题组对对照组及经过24小时吗啡处理的膀胱癌T24细胞进行全转录组测序。测序结果提示,细胞连接、细胞粘附、细胞迁移,以及上皮-间质转换等信号通路被显著富集。课题组通过体外细胞研究进一步证实,经过吗啡处理后的T24细胞发生显著间质化形变,且细胞运动、侵袭迁移,以及形变能力均大大增加。

图3
MORAs显著促进膀胱癌细胞发生上皮间质转化。
3.MORAs通过上调转录因子Slug促进膀胱癌细胞发生EMT。
课题组通过对介导EMT的关键转录因子进行分析发现,MORAs会显著上调Slug的表达。通过敲减Slug能够明显抑制EMT的发生,且削弱膀胱癌细胞侵袭迁移能力。在体小鼠皮下瘤模型也证明,抑制Slug会显著抑制肿瘤生长,有效逆转MORAs导致的间质型CTCs及间质型CTCs簇数量增加。

图4
MORAs通过上调转录因子Slug促进膀胱癌细胞发生上皮间质转化。
4.MORAs通过激活膀胱癌细胞中MOR/PI3K/AKT信号通路上调Slug。
课题组首先通过生信分析发现,Slug与AKT信号通路关系密切。随后体外及在体实验均证实MORAs可显著激活PI3K/AKT信号通路,且通过阻断该通路可有效逆转MORAs导致的EMT。此外,细胞实验及在体肿瘤模型均发现,敲减MOR会显著逆转MORAs导致的EMT,并抑制膀胱癌生长。

图5
MORAs通过激活MOR/PI3K/AKT信号通路促进膀胱癌细胞发生上皮间质转化。
5.围术期MORAs使用增加膀胱癌患者术后血液中CTCs的数量。
为了进一步探讨MORAs使用与CTCs形成之间的关系,课题组在上海交通大学医学院附属仁济医院开展了“围术期阿片类药物应用对达芬奇机器人辅助下膀胱癌根治性切除术患者术后循环肿瘤细胞数目影响”的临床前瞻随机对照试验。符合入排标准的接受膀胱癌根治性切除术的患者被随机分配到全麻组或全麻+硬膜外麻醉组,其中全麻+硬膜外麻醉组患者围术期使用的MORAs的总量较常规全麻组大大减少。通过分析每位患者术后不同时间点血液中CTCs的数量,课题组发现,与全麻组患者相比,从术后3天起,全麻+硬膜外麻醉组患者血液中多种类型CTCs数量均明显更低,且差异可维持到至少术后一个月。

图6
围术期MORAs使用增加膀胱癌患者术后血液中多种CTCs的数量。
主要作者简介
通讯作者

田婕
上海交通大学医学院附属仁济医院
个人简介
田婕,博士,副主任医师,硕士研究生导师,上海交通大学医学院附属仁济医院麻醉科科副主任,上海市医学会麻醉学分会青年委员会副主任委员。长期从事麻醉对肿瘤转归的影响方向的研究,在美国UT MD Anderson Cancer Center有过4年多博士后研究经历。在相关领域以第一作者和通讯作者在the Journal of Clinical Investigation等国际知名期刊上发表SCI文章近30篇,累计影响因子>150分。以项目负责人承担国家自然科学基金和上海市自然科学基金等多项国家和省部级课题。

俞卫锋
上海交通大学医学院附属仁济医院
个人简介
医学博士、主任医师教授、博士研究生导师
中国医师协会麻醉学医师分会第四届委员会会长
中华医学会麻醉学分会副主任委员
现任上海交通大学医学院附属仁济医院麻醉科主任
上海交通大学医学院麻醉与危重病医学系主任
中华医学会麻醉学分会儿科学组组长
上海市医学会麻醉专科委员会第九届委员会主任委员
担任《麻醉.眼界》、《Anesthesiology》中文版主编,《中华麻醉学杂志》、《临床麻醉学杂志》、《APS》副总编辑。主持9项并指导科室国家自然科学基金79项,获国家自然科学基金生命科学部重点课题和科技部重大研发计划各一项。以第一负责人承担30项省部级以上课题,主编专著11部。共发表论文300余篇,SCI收录140篇,总IF>400分。有多篇发表在JCI、Anesthesiology、Advanced Science、BJA、Pain、Stroke、Science Translational Medicine、Nature Communications、ACS-NANO等著名杂志上。获国家和军队科技进步二等奖各一项,教育部科技进步奖一等奖一项。另获总后勤部“科技新星”、上海市卫生系统“银蛇奖”、军队院校“育才奖”银奖、“上海市优秀学科带头人”、“上海市科技精英提名”等各种奖励。

杨朝勇
上海交通大学医学院附属仁济医院
个人简介
上海交通大学分子医学研究院,教授、副院长
厦门大学化学化工学院,教授、博士研究生导师
中国化学会化学生物学专业委员会副主任、谱学分析与仪器教育部重点实验室副主任
担任ACS Applied Bio Materials 副主编; BMC Biochemistry 副主编、Analytical Chemistry、Lab on a Chip、Analyst、Talanta等期刊编委/顾问编委。近年主持主要科研项目包括:国家重大科研仪器研制项目、科技部国家重点研发计划合成生物学专项课题、国家自然科学基金委重点项目、国家杰出青年科学基金、科技部973课题、科技部国家重大科学仪器设备开发专项子任务等。
先后获得福建省杰出青年基金、国家杰出青年科学基金、福建省高校领军人才、福建省科技创新领军人才、厦门市双百计划领军型创业人才、福建省自然科学优秀学术论文一等奖、中国青年分析化学家奖、中国化学会-英国皇家化学会青年化学奖、科技部中青年科技创新领军人才、中组部等9部委《全民科学素质行动计划纲要》实施工作先进个人、福建省科技进步一等奖、美国化学会测量科学进展讲座奖等奖项与称号。主要研究方向为:体外诊断新方法,创新仪器,微流控技术在生物医学中的应用,单细胞分析,纳米生物医学工程,功能化DNA纳米组装。

曹明
上海交通大学医学院附属仁济医院
个人简介
仁济医院泌尿科副主任医师,2002年毕业于原上海第二医科大学临床医疗系,后先后师从黄翼然教授及薛蔚教授,分别在硕博期间从事遗传性肾癌及膀胱癌的基础及临床研究,临床工作以原位新膀胱手术及保留膀胱治疗为特色,同时在膀胱癌液态活检、免疫治疗及肿瘤代谢领域开展了多项基础及转化研究。在Eur Urol等杂志发表论著20余篇,拥有发明专利一项。学会任职包括CUDA数字与人工智能学组专委会委员,上海中西医结合学会智慧医疗与人工智能专委会委员,上海泌尿外科质控中心专委会秘书兼督查专家等。
(来源:CancerCommunications)
声明:古麻今醉公众号为舒医汇旗下,古麻今醉公众号所发表内容之知识产权为舒医汇及主办方、原作者等相关权利人所有。未经许可,禁止进行转载、摘编、复制、裁切、录制等。经许可授权使用,亦须注明来源。欢迎转发、分享。
本文转载自其他网站,不代表健康界观点和立场。如有内容和图片的著作权异议,请及时联系我们(邮箱:guikequan@hmkx.cn)
本文来自投稿,不代表长河网立场,转载请注明出处: http://www.changhe99.com/a/V5daDjbVwX.html

