作者:医学镜界
特发性草酸钙 (CaOx) 结石形成者 (ICSF) 与特发性磷酸钙 (CaP) 结石 (IPSF) 的患者不同。ICSF,但不是IPSF,在间质磷灰石斑块上形成过度生长的结石;覆盖乳头状表面的斑块量与尿钙排泄呈正相关,与尿量成反比。斑块的数量预测复发性结石的数量。斑块上最初的晶体过度生长是CaP,尽管结石主要由CaOx组成,这意味着降低CaOx和CaP的过饱和度(SS)对于预防CaOx结石很重要。与 ICSF 不同,IPSF 在髓质内集合管中具有磷灰石晶体沉积物,这与间质瘢痕形成有关。ICSF和IPSF有特发性高钙尿症,这是由于小管钙重吸收减少,但重吸收异常的部位可能不同。近端小管 (PT) 重吸收减少将更多的钙输送到粗支升段 (TAL),钙重吸收增加会加重间质,导致斑块形成。IPSF中异常重吸收的部位可能是TAL,其中碳酸氢盐重吸收的相关缺陷可能产生IPSF较高的尿液pH特征。通过液体摄入、蛋白质和钠限制以及噻嗪类药物进行预防性治疗将通过降低尿钙浓度以及 CaOx 和 CaP SS 对 ICSF 和 IPSF 有效,并且还可以通过增加 PT 钙重吸收来减少斑块形成。如果尿液pH值大幅升高,增加CaP SS,柠檬酸盐可能对IPSF有害。未来的试验应检查IPSF的适当治疗问题。
介绍
到目前为止,从改变尿液过饱和度和结晶抑制剂的角度来看,减少饮食钠和蛋白质、增加液体、噻嗪、柠檬酸钾、减少饮食嘌呤和别嘌呤醇的常见措施。在这里,我们在这个熟悉的主题上增加了关于石头如何实际形成以及驱动其形成的机制如何实际运作的新工作。其结果是对使用公认的治疗方法的理解达到了一个新的水平,这应该给医生及其患者带来更大的信心和微妙的管理。
这项新工作不仅根据临床外观,而且根据肾脏病理学划分了钙结石形成者。我们一直将因全身性疾病而形成钙结石的患者与特发性钙结石形成者区分开来。然而,我们现在知道,结石主要是草酸钙的特发性钙结石形成者与结石不是草酸钙的特发性钙结石形成者明显不同。这种新的区别具有真正的临床效果,需要新的试验。
特发性草酸钙结石形成者
石头生长在间质磷灰石(斑块)沉积物上
在最常见的患者中,钙结石不是由全身性疾病引起的,而是“特发性的”。其中,大多数( 1 )形成结石,其中最丰富的晶体是草酸钙(CaOx)。特发性 CaOx 结石形成者 (ICSF) 的肾脏正常,但状间质磷灰石沉积物 ( 2 , 3 ) 显示为白云 ( 图 1A )在输尿管镜检查(URS)或经皮肾镜取石术(PERC)期间尿路上皮下。肾结石生长在这些沉积物上,通常称为“白色斑块”,位于的外部( 图1B ).上皮隔室内未见晶体( 4 )。沉积物没有引起明显的炎症,肾外观完全正常,除了斑块和过度生长的结石。
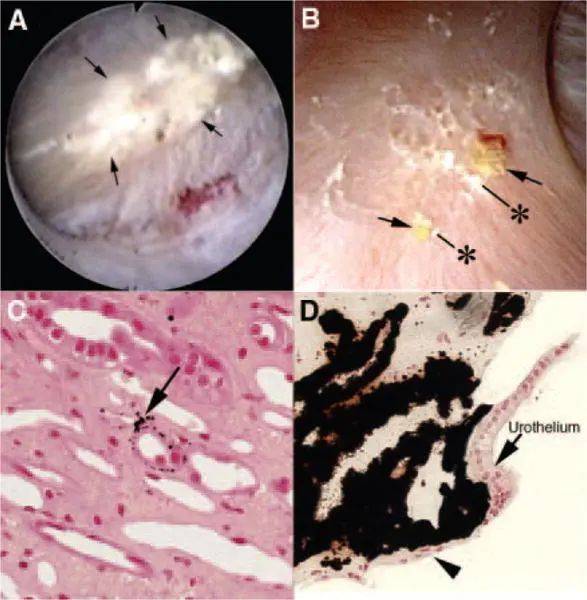
图1 特发性草酸钙结石形成者(ICSF)间质斑块的内镜和组织学特征
(A)来自ICSF的示例,该在映射协议时被视频录制。状尖端被不规则白色物质(箭头)的多个部位覆盖,称为“间质”或“兰德尔斑块”,可通过尿路上皮覆盖物看到。这些斑块区域是结石附着的部位。(B)看到两块约0.5毫米的小石头(星号)与间质斑块(箭头)区域有关。与间质斑块部位相邻的状活检的组织学检查显示,结晶物质(C中的箭头)最初积聚在Henle细环的基底膜中。随着时间的推移,这些小的沉积物部位似乎积聚在间质空间中,作为密集的矿物质岛进入肾尿路上皮覆盖物的基底表面(D中的箭头)。改编自参考文献 2 , 8 。
斑块开始于微小微球的集合,这些微球在Henle环( 图1C ),并从那里扩散到间质,最终在内髓质集合管 (IMCD) 和贝里尼 (BD) 末端导管的尿路上皮和基底膜下方,在那里它们表现为白色斑块( 图1D ).
在一项针对 ICSF 的前瞻性研究中,使用 PERC 观察的所有结石均被分类为附着或不附着,而附着的结石进一步分类为附着或不附着斑块 ( 5 )。大多数石头都附着在斑块上,其中所有石头都附着在斑块上,或者无法完全验证其附着部位。验证要求术中分类与术后数字视频记录的分类一致。尽管在验证方面存在一些困难,但结果压倒性地支持这样的假设,即依恋是规则,依恋几乎总是在斑块上。在对未附着的结石的后续研究中,发现大多数具有磷灰石表面病灶,可能是对间质斑块的附着物( 6 )。这项工作的主要含义是斑块对结石的形成至关重要,如果是这样,斑块丰度和复发结石的数量应该相关;事实上,他们确实如此,这一发现加强了石块与石匾的联系( 7 )。
由于ICSF中的CaOx结石生长在肾单位外和斑块上,临床医生的主要问题是减少过度生长(给定斑块)以及预防斑块本身。直到最近,我们一直将我们的治疗仅用于第一个目的;我们现在有理由在临床范围内考虑这两个目的。
斑块的形成
尿液危险因素
斑块覆盖的乳头状表面部分随尿钙而变化( 8 ),随尿量和pH值( 图2 ).从所有三个测量得出的多变量评分占ICSF和正常对照之间斑块丰度变化的很大一部分。对于临床医生来说,这意味着高尿量和控制尿钙,这两种谨慎的结石减少手段,也应该有利于斑块的形成。
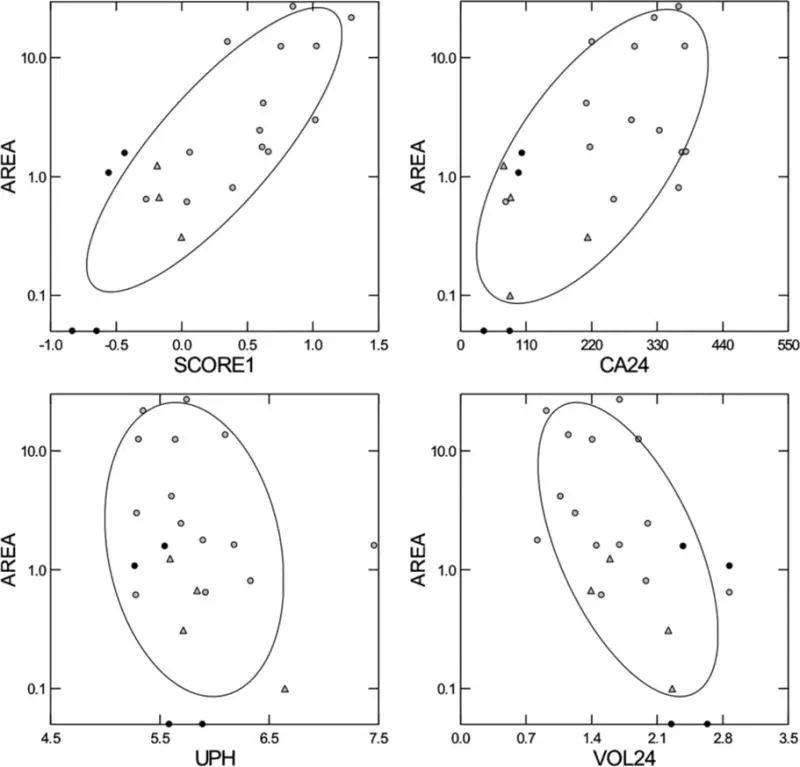
图2 斑块丰度与尿液发现之间的关系
根据术中数字成像(所有四个面板的 y 轴)确定,斑块覆盖的乳头状表面部分随尿钙(右上图)而变化,与尿液 pH 值和体积(下图)成反比。使用所有三个变量的多变量评分占斑块覆盖率的大部分变化(左上图)。○, ICSFs;● 控制;△'肥胖旁路手术患者。评分1、体积钙pH评分;Ca24,尿钙(毫克/天);UPH,尿液pH值;VOL24,尿量(升/天)。改编自参考 文献8 。
尿液发现与斑块之间的生理学联系
这些尿液因素如何影响斑块需要更深入地研究所涉及的肾脏生理学,而这种观察增加了临床管理的细微差别和微妙之处。在中,细肢段各被三到四个毛细血管包围( 图3 ,下面板)。由于水的重吸收,细肢段液的钙浓度超过血液水平( 9 ),但上皮细胞具有非常低的钙通透性,根本不运输钙 。即便如此,细肢段液总是与其上皮接触,因此钙必须以比血液更高的浓度进入基底膜,特别是在不允许大量水流动的上升部分。然而,基底膜的外侧会以与间质液的钙摩尔浓度成反比的速度将钙运输到周围的间质中,并且摩尔浓度将不可避免地由输送到毛细血管的血液的钙浓度主导。
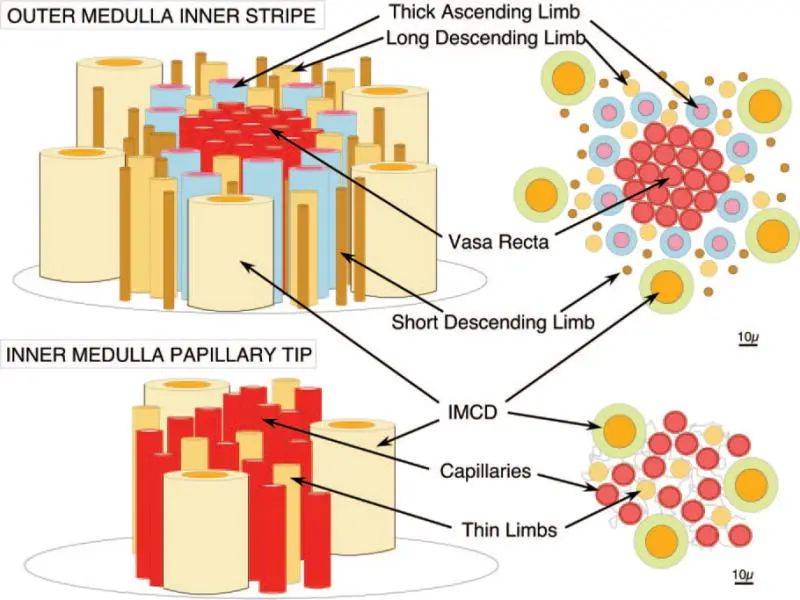
图3肾 髓外和肾乳头尖端示意图
Vasa 直小血管通过外髓质的内条纹成束下降,周围环绕着厚厚的升肢粗段环。在肾乳头尖端,斑块在细肢的基底膜中形成,细肢各被三到四个毛细血管包围,这些毛细血管来自下降的直小血管。
血液在下降的直小血管中下降,在外髓质的内条纹中形成束,周围环绕着一圈厚实的上升肢体( 11 ) ( 图3 ,上)。粗升肢主要通 过钠-钾-氯化物共转运蛋白 2 和肾外髓质钾通道产生的腔阳性跨上皮电位重吸收钙而无需水。 .无水输送钙必须用钙富集内条纹间质,这反过来又必须提高降血管直小血管中血液的钙浓度。因此,在所有条件下,细肢段的基底膜将在两侧被钙浓度高于血液的液体沐浴:腔液通过水提取,组织液通过血管冲洗。
这可能解释了为什么即使在正常人中也会形成间质斑块并在这个特定部位开始;然而,到目前为止,我们还没有解释为什么ICSF中的斑块比正常人更丰富,因为细肢和厚肢段的解剖结构和功能基本相似。
特发性高钙尿症
关键区别在于 ICSF 中的钙管理方式与正常人不同。男性和女性人群表现出广泛的尿钙排泄范围,从每天低至<50至高至>500毫克,男女的平均值在每天130至170毫克之间( 12 )。ICSF似乎是从该分布的高尾中选择的,因为它们的平均值是正常个体的两倍。像身高一样,钙排泄似乎是由遗传决定的,因为高值在家庭中运行( 13 ),并且可以为此繁殖啮齿动物( 14 )。如此高的尿钙排泄不是一种疾病,而只是高钙血症人群结石风险高的原因。据说ICSF患有特发性高钙尿症(IH),但考虑这个问题的更好方法是,它们只是从人类正常遗传禀赋的一端抽取的。
在人类和动物中,IH反映了组织维生素D活化增加:肠道钙吸收和骨矿物质动员增加,低钙饮食可导致负骨矿物质平衡( 13 )。但这里感兴趣的是比正常情况下更多的钙进入尿液。它可能来自血钙增加,因为每餐中的钙以异常快的速度吸收;它可能来自小管钙重吸收减少。事实上,它是后者( 15 )。吃固定和相同的高钙和正常饮食,ICSFs与IH一起减少每餐的总小管重吸收超过匹配的对照组,因此在相同的血清钙水平和钙过滤负荷下,它们排泄更多的钙。
这不足以解释ICSF中的斑块高于正常值,除了我们补充说,使用内源性锂清除作为标志物,近端小管参与整体小管钙重吸收的减少( 16 ),因此,钙输送到细肢异常高( 图4 ).在此图中,每个点代表在一般临床研究中心的三餐日中以ICSF(黑色圆圈)或对照组(灰色圆圈)进行的15个清除期。与对照组相比,ICSF远端输送的钙要多得多,尿钙排泄与远端输送相当相似。
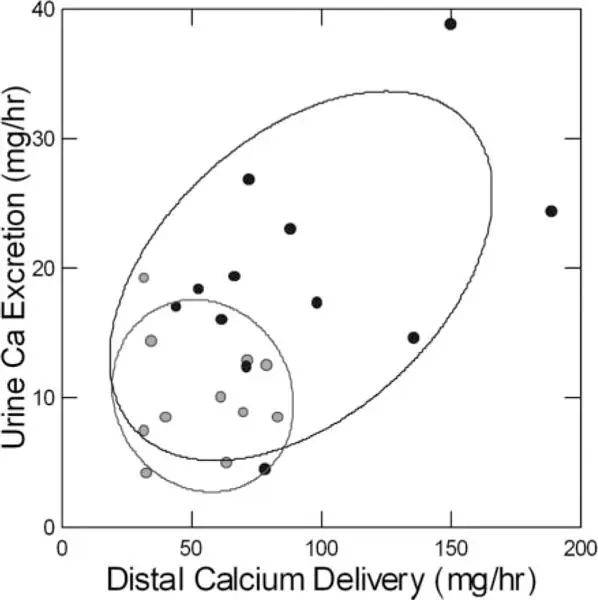
图4 尿钙排泄( y 轴)与近端小管钙输送( x 轴)之间的关系
在ICSF(黑色圆圈)中,尿钙排泄随着近端小管远端输送而增加,而匹配对照受试者的值聚集在左下象限(灰色圆圈)。每个点是综合临床研究中心一日三餐15个清除期的平均值;受试者都吃同样的饮食。使用内源性锂清除率测量近端重吸收。改编自参考 文献45 。
细肢不能明显地重吸收钙,因此远端输送的增加意味着增加的钙进入厚实的升肢,在那里它主要通过原力被重新吸收。这意味着更多的输送通常会导致相应的更多重吸收,没有水,进入内髓质外条纹的间隙。反过来,下降的直肠血管会更预先加载钙,的毛细血管会更大程度地富含钙,从而促进薄肢基底膜中的晶体成核。从最广泛的意义上讲,人们会期望斑块丰度与尿钙排泄平行,它确实如此。当然,如果要正确测试这一假设,则必须测量人体组织中的间质钙浓度;这样的测量是可以进行的,我们希望研究人员将这个特定的测试作为研究目标。未能发现间质钙的增加将推翻我们的假设。
尿量对斑块的影响
该模型还预测斑块丰度通常与尿量成反比。加压素是髓质厚升肢运输的主要激动剂,通过 V2 受体起作用,当尿量低时最高,反之亦然。此外,高尿流量引起的髓质冲洗往往会降低所有乳头状间质溶质(包括钙)的浓度。
此模型的局限性
我们将这项工作呈现为正在进行中且有价值的,因为它会导致进一步的测试。例如,锂清除率不是近端小管重吸收的直接测量值,并且可能会产生误差。其他检查(例如,呋塞米阻断厚升肢后尿钙增加)将是有价值的确认( 17 ),游离水清除率的研究也可能是有价值的证实。同样 图4 清楚地表明,并非所有ICSF都显示出相同程度的近端小管改变,但我们目前无法将近端重吸收与斑块丰度测量相关联。后一种比较将是对我们提出的假设的关键测试,可以在人类受试者中进行。
可减少斑块形成的临床措施
由于除手术外无法在患者中量化斑块,因此用于预防牙菌斑的随机对照试验(RCTs)尚不实用,但从我们已经介绍的内容中,临床医生可以得出一些合理合理的方向,这些方向没有风险和高潜在益处。
减少饮食钠和蛋白质,长期以来一直提到适度高钙尿症( 18 ),可能会增加近端小管重吸收。第一种作用于减少细胞外液体积。第二种减少蛋氨酸和胱氨酸上硫氧化产生的内源性酸;酸负荷减少近端重吸收( 19 )。噻嗪类利尿剂是结石预防的主要药物( 20 ),因为它们可降低尿钙排泄。在啮齿动物中,可能还有人类,它们通过减少细胞外液量来增加近端重吸收( 21 )。高水摄入量是RCTs支持的明显结石预防( 22 ),将减少加压素,从而减少髓质厚升肢重吸收( 23 ),并促进髓质溶质冲洗。对于尽管采取了所有其他措施,结石仍复发的患者,人们可能会考虑每晚一次夜尿,因为尿量最低,加压素可能在一夜之间最高。
仅经过一块结石后,我们建议仅进行适度的治疗( 24 ),但人们可能会认为,在ICSFs制造结石之前需要形成斑块,并且结石复发倾向于与斑块丰度平行( 7 )。鉴于这一点,在结石病的自然史中,尽快进行高液体和减少饮食蛋白质和钠是合理的,这意味着与第一块结石。
即使在第一块结石时,并且通常在疾病过程中,外科医生也可以通过URS或PERC获得至少对斑块丰度的粗粒度视觉评估。我们看到了要求外科医生与我们分享他们的最佳印象的所有好处。鉴于存在大量斑块,最好尽可能推动结石预防工作,并使患者意识到更高的潜在复发风险。后者可能会增加他们维持预防治疗的愿望,特别是与饮食和液体摄入有关的治疗。
结石如何在斑块上生长
在 1 mm CaOx 结石 ( 图5 )斑块沉积物上的尿路上皮被破坏,斑块表面暴露于尿液中( 25 )。暴露的表面被尿液来源的有机物质的内部边界密封,含有Tamm-Horsfall蛋白和骨桥蛋白以及其他分子。磷灰石晶体在层中成核,被较多的有机基质覆盖,发生新的成核,最终晶体层和有机层交替形成层状带状。当结晶扩散到形成石基的尿腔时,丝带终止。在这张透射电子显微照片中,斑块在左下角,白色箭头显示内部边界层,晶体在石头底部用星号和双箭头显示。插图显示了碳带及其晶体在较高放大倍率下的细节。
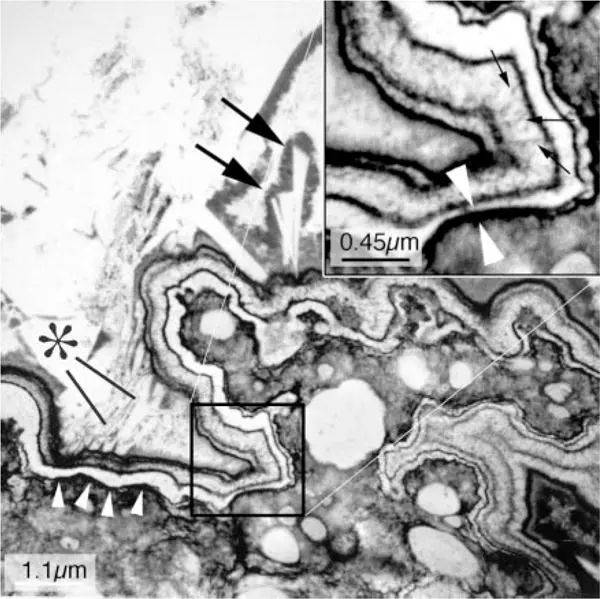
图5 草酸钙(CaOx)结石附着部位的透射电子显微镜图像
这张高放大倍率的显微照片显示了斑块-结石界面的超微结构特征。显微照片的左上角显示了尿腔中的结石物质,而右下角显示了肾中的间质斑块区域。由一排四个箭头表示的斑块边界具有多层丝带的外观。当放大该色带中由正方形标记的部分时(见右上角的插图),可以看到这种丝带状结构具有九个独立的层,其中五个薄的黑色有机薄片与四个白色薄片交替出现。在最厚的白色薄片中,人们可以看到垂直于表面的微小针状体,并具有多个空隙的外观,其中包含紧密排列的晶体(插图中的小箭头)。插入物中看到的两个白色箭头标记了最接近肾组织的黑色薄片。星号标记了一系列小晶体,而两个大箭头标记一组较大的晶体,这些晶体似乎插入了色带的最外层(泌尿侧)。所有晶体材料似乎都被黑色基质材料覆盖。改编自参考 文献25 。
除了斑块本身的形成外,该过程的关键步骤是尿路上皮的破坏,我们目前对此一无所知,以及最初的磷灰石成核,这推动了新结石的形成。这种成核完全取决于尿磷酸钙(CaP)过饱和度(SS),这意味着即使在CaOx结石形成者中,CaP SS也是需要尽可能控制的关键临床变量。
在ICSF中,CaP SS远远超过正常( 图6 ,右下面板),甚至比CaOx SS( 图6 ,右上方面板)。平均而言,正常人不会达到CaP SS值>1,这意味着最初的磷灰石成核可能确实很少见,而ICSF中的值几乎一直都是>1( 26 )。对于ICSFs,CaP SS的最高值是下午晚些时候和夜间,此时正常人的SS适度下降。高 CaP SS 由高尿钙摩尔浓度 ( 图6 ,左上图),本身起源于 IH,但尿量没有任何相应的增加( 图6 ,中下面板)。ICSF和正常个体( 图6 ,左下面板)。
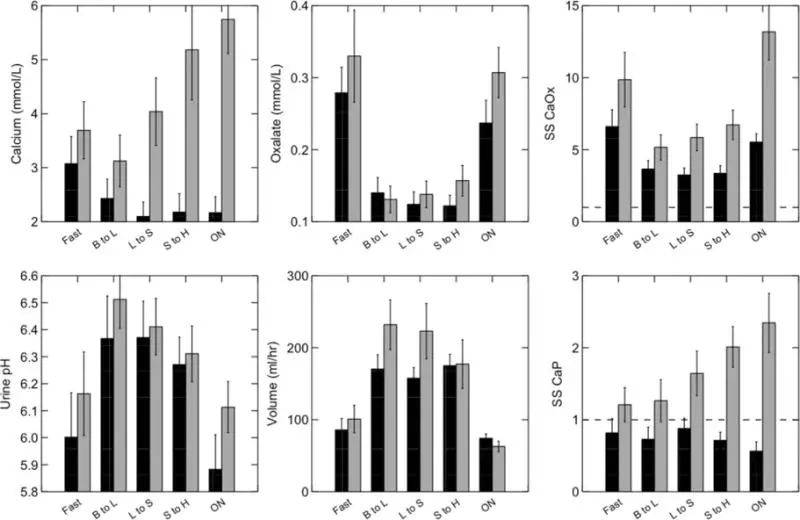
图6 ICSF(灰色条)和正常对照组(黑条)中三餐一天的尿磷酸钙 (CaP) 和 CaOx 过饱和度 (SS)
受试者都吃相同的饮食,并在禁食期间使用15种尿液进行研究,从早餐到午餐(B到L),午餐到晚餐(L到S),晚餐到家(S到H)和过夜(ON)。ICSF的CaP SS(右下图)在一天的最后三个时段超过了正常对照,正常对照从未达到平均SS >1(水平虚线)。高CaP SS的主要原因是尿钙摩尔浓度(左上图),其本身是由高钙尿症引起的,而没有伴随尿量增加(中下图)。尿液pH值无显著差异(左下图)。ICSF的尿CaOx SS超过正常对照组(右上图),主要是因为钙摩尔浓度较高;尿草酸盐摩尔浓度没有差异(中上图)。改编自参考 文献46 。
ICSF的尿量并不比正常人高,这肯定是奇怪的,因为顶端集合管钙受体(CaSR)应该感知钙摩尔浓度上升并减少水重吸收;然而,事实只是说这不会发生。例如,过夜,ICSF之间的钙摩尔浓度接近6 mM,而正常为2 mM,但尿量相同。CaSR可能是保护性的,但仅在尿钙排泄水平较高的情况下。在体外研究的人CaSR在尿液的pH和离子强度下钙离子摩尔浓度为6时受到一半刺激,但在人尿液中,总钙摩尔浓度为6意味着仅约3mM钙离子。剩余的尿钙结合在有助于产生SS的复合物中,例如磷酸盐和草酸盐。因此,在我们的患者中缺乏效果实际上与人们的预期并没有不同。
可减少斑块结石过度生长的临床措施
即使在ICSF中,减少CaP SS可能与减少CaOx SS一样重要。高尿量应该有帮助,所有减少尿钙的措施,包括减少饮食中的钠、蛋白质和噻嗪类药物。一夜之间是高CaP SS的时期,1×夜尿症在难治性患者中可能很重要。换句话说,治疗方法与斑块相同。
然而,枸橼酸钾是复杂的,如果可能具有价值。碱通过减少饮食净酸负荷减少尿钙排泄并增加近端小管重吸收( 27 ),两项RCTs记录了钙结石形成者伴有低枸橼尿症的益处,其中ICSF在统计学上占主导地位( 20 )。柠檬酸盐是磷灰石成核和生长的极好抑制剂( 28 , 29 );然而,柠檬酸盐可以提高尿液pH值和CaP SS,因此我们认为谨慎的做法是剂量足以将尿氨减少一半至三分之二;更多几乎肯定会提高pH值。例如,以毫摩尔/天为单位的初始剂量可能是尿氨的一半到三分之二,以毫摩尔/天为单位,源自标准的市售 24 小时尿肾结石风险小组。
尿草酸盐在任何ICSF中都远非微不足道,因此即使在这个以CaP为导向的讨论中,我们也注意到,即使使用固定和相同的饮食,ICSF中的草酸盐排泄也高于正常水平,并且CaOx SS也更高,尤其是隔夜( 30 )。此外,与吃相同饮食的正常对照受试者相比,ICSFs经常表现出肾草酸盐分泌( 31 ),这表明可能促进CaOx结晶的新机制。降低CaOx SS应减少CaOx在新CaP结石病灶上的体积成核和生长,因此非常重要。尿草酸盐排泄率>45 mg/d通常来自可以纠正的低钙或高草酸盐饮食。>65-70mg/d的值可能反映原发性高草酸尿症或肠道高草酸尿症( 20 )。没有随机对照试验支持减少尿草酸盐作为ICSF的治疗方法。
最后,高尿酸尿症可能通过盐析降低CaP和CaOx的溶解度,从而提高两种成核的倾向( 32-34 )。这也许就是为什么使用别嘌呤醇的单一RCT如此积极的原因( 35 )。减少饮食嘌呤也应该这样做,但尚未进行试验。
随机对照试验符合斑块形成和过度生长的模型
在一项针对男性ICSFs的RCT中,低钠和低蛋白饮食在减少结石方面比低钙饮食更有效,低钙饮食不会增加近端小管重吸收( 18 )。所有三项全把握度的3年噻嗪类药物试验( 36-38 )均呈高度阳性,两项在低柠檬酸性钙结石形成者中使用枸橼酸钾的RCTs( 39 , 40 )和一项在高尿酸排泄性钙结石形成者中使用别嘌呤醇的RCT也是如此。噻嗪类、柠檬酸盐和别嘌呤醇RCT涉及特发性钙结石形成者,其中ICSF一定占主导地位,但肯定也存在一些CaP结石形成者。
ICSF有特定的疾病
因为IH可以通过已知的肾脏解剖学和生理学与斑块联系起来,因为它们的结石通过一系列明确的成核在斑块上生长,并且因为IH本身的机制和起源也越来越为人所知,所以IH的结石病可以从其病因,通过其发病机制到其最终的组织表达来理解。鉴于最后的疾病,结石,可以用机械术语很好地解释,ICSF似乎满足矿物质代谢凝聚性疾病的合理标准。我们在离开这个主题时注意到,一代人的研究已经确定了尿液抑制钙晶体成核和生长的显着能力( 41 );抑制异常很可能是ICSF表型的一部分,但这方面的证据充其量是很少的,在问题具有临床相关性之前,必须做更多的工作。
特发性 CaP 结石形成者
特发性 CaP 结石形成者 (IPSF) 的结石含量为 >50% 与 ICSF 截然不同,以至于它们的结石很可能来自完全不同的病因和发病机制。无论他们在表面分析上多么类似于ICSF,他们都没有这种疾病。相反,他们的肾脏参与了更具破坏性的局部过程。IPSF可以形成磷灰石或刷石(磷酸一氢钙)的结石;到目前为止,我们只有后一组的数据,即brushite IPSF,以下内容仅适用于它们。
IPSF用磷灰石晶体插入BD和IMCD
在PERC或URS期间,存在白色斑块( 图 7A ,箭头);显示瘢痕区域(箭头)和散布的巨大扩张BDs,上面塞有磷灰石晶体,通常从导管开口突出( 42 )并伸入尿腔(星号)。活检( 图 7,B 到 F )受影响的BD可以扩张20倍;上皮细胞缺失(箭头)。受影响的BD周围有间质纤维化(图例详细说明了每个面板中的变化)。晶体介导的损伤基本上会导致局灶性状肾小管间质性肾病。
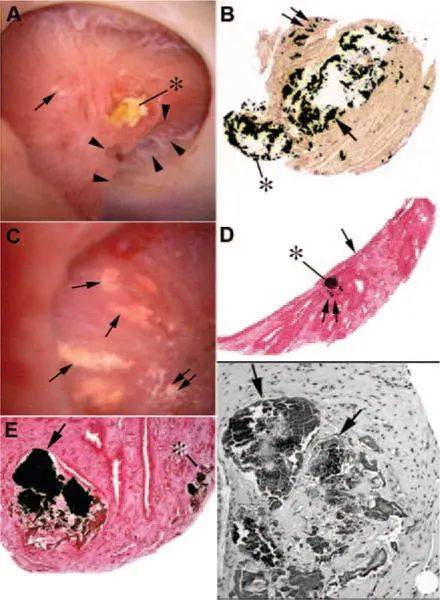
图7结 石患者晶体沉积的内镜和组织学图像
结石形成者的的内镜检查揭示了从正常到严重畸形的各种病变。(A)具有广泛凹陷的,其特征是一系列箭头和Bellini导管远端(BDs)的广泛扩张,通常充满突出的结晶塞(星号)。兰德尔斑块的小区域(A中的单箭头)被称为“1型晶体图案”是常见的。状活检的组织学检查显示,尿腔内髓质集合管 (IMCD) 和 BD(B 中的箭头)极度扩张,矿物质偶尔突出(B 中的星号)。可见间质斑块部位(B中的双箭头)。其他具有兰德尔斑块(C中的双箭头)和黄色斑块区域(C中的单箭头)的部位,称为“2型晶体图案”。黄色斑块的每个部位在方向上都是线性的,当多个这样的区域彼此靠近时,它们形成辐条和轮状图案(C)。对黄色斑块单个部位的组织学检查显示,这些区域代表充满矿物质(D中的星号)的IMCD,位于尿路上皮覆盖物正下方(D中的单个箭头)。D图的双箭头标记了兰德尔牌匾的位置。对Yasue染色切片的光学显微镜检查显示,堵塞的IMCD含有大量矿物质(E中的箭头),这些矿物质填充了严重受损小管的管腔,而附近的小管看起来正常。在Henle的细环中也发现了矿床(E中的星号)。用血毒素和伊红染色的组织切片显示嵌入间质纤维化区域的晶体填充的IMCD(F中的箭头)。改编自参考 文献42 。
堵塞和高结石CaP丰度的机制似乎只是高尿CaP SS( 43 )。平均尿钙SS( 图8 ,左图)的钙结石形成者随着分析的结石中磷酸盐比例的增加而平稳增加( 图8 ,两个面板的 x 轴)。这是因为尿液pH值升高( 图8 ,右面板)。pH值升高的原因尚不清楚。这些地块上的所有患者组均具有等效的 IH。由于IMCD和BD小管液接近最终尿液,因此两个部位的CaP SS必须更高,从而导致散发和破坏性结晶。
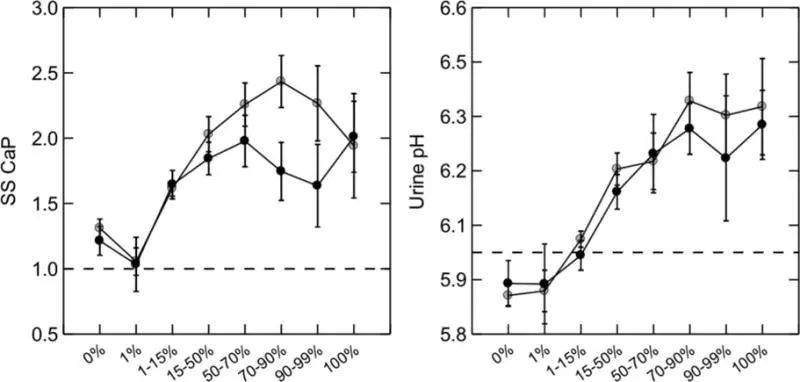
图8 结石形成者尿CaP SS和pH值随着结石CaP丰度的增加
钙结石形成者按所有分析结石中的CaP百分比分组(x轴)。CaP SS(左图,y 轴)随着宝石中 CaP 百分比的升高而逐渐上升;主要原因是尿液pH值逐渐升高(右图,Y轴)。尿钙和磷酸盐排泄量(未显示)在结石百分比类别中没有变化。女性(灰色圆圈)和男性(黑色圆圈)表现出基本相同的行为。改编自参考 文献43 。
IPSF中较少的斑块引发了重要的研究问题
与 ICSF 相比,IPSF 的尿钙排泄量略高,尿量大致相同,但 pH 值越高,表明斑块较少。输精管冲洗对两组的操作方式应相同。然而,至少有两种替代机制可以减少斑块。与ICSF相比,IPSF中IMCD中的净质子分泌会减少,这将减少碳酸氢盐进入状间质,从而降低间质液pH值。较高的pH值将促进薄环基底膜中的CaP成核。
或者,与 ICSF 相比,髓质厚升肢可能减少了 IPSF 的绝对钙重吸收。尽管两者都表现出相同的尿钙丢失,甚至减少了整体小管重吸收变化,但IPSF不会像ICSF中那样在直肠血管中加载钙。由于厚实的升肢重吸收约15%的过滤碳酸氢盐( 44 ),因此减少重吸收将增加远端碳酸氢盐向IMCD和BD的递送,提高那里的pH值并促进CaP结晶。换句话说,IH可能有几个小管表达,一个主要集中在近端小管,一个在厚厚的上升肢体中,可能在这两个极端之间有一个频谱。在近交高钙尿症大鼠中,近端小管和厚升肢钙重吸收异常低( 17 )。因此,IPSF与ICSF中肾单位生理学的比较为新的人类发现提供了非凡的机会。
IPSF的管理
减少饮食钠和蛋白质以及高液体摄入量和噻嗪的价值与ICSFs相同 - 不同的是柠檬酸钾的作用。如前所述,柠檬酸盐是CaP成核和生长的抑制剂,但如果尿液pH值和CaP SS升高,结石和堵塞就会增加。对于这种确切的患者,迫切需要RCT。鉴于IPSF并不罕见,这项试验早就应该进行了。
人们不必等待结石分析。任何URS或PERC都是外科医生观察堵塞的机会,这在ICSF中是不存在的。为我们的患者服务的泌尿科医生应始终被询问是否看到堵塞,以及是否可以粗略估计堵塞和状回缩和疤痕的数量。
总结
从结石形成者肾的手术活检中得出的信息正在改变我们对钙结石形成方式的理解。斑块在CaOx结石形成中的重要性意味着减少牙菌斑形成的方法应成为预防结石的目标。CaP SS在CaOx和CaP结石形成中的作用意味着降低CaP SS应该是ICSF和IPSF的目标。ICSF和IPSF之间的显着组织病理学差异突出了需要一项试验来评估每组结石预防的治疗方法。随着我们对结石形成的病理生理学的理解提高,它将为我们为患者选择适当治疗方法的能力提供信息。
Coe FL, Evan A, Worcester E. Pathophysiology-based treatment of idiopathic calcium kidney stones. Clin J Am Soc Nephrol. 2011 Aug;6(8):2083-92. doi: 10.2215/CJN.11321210. PMID: 21825103; PMCID: PMC5825183.
本文转载自其他网站,不代表健康界观点和立场。如有内容和图片的著作权异议,请及时联系我们(邮箱:guikequan@hmkx.cn)
本文来自投稿,不代表长河网立场,转载请注明出处: http://www.changhe99.com/a/yBrgZ58k6P.html

